- はじめに
- Genome organization / ゲノム構造
- Viral structural proteins / ウイルス構造タンパク質
- Essential regulatory elements / 必須の規制要素
- Accessory regulatory proteins / アクセサリー制御タンパク質
- RNA secondary structure / RNAの二次構造
- V3 loop / V3ループ
はじめに
この記事は、2021年12月13日現在のWikipedia 英語記事「Structure and genome of HIV」を日本語翻訳したものである。
この情報は、Wikipediaの英語ページのみにあり、まだ日本語ページは存在していません。結構しっかりした内容で発信するのに有用だと思いましたので、このwikipedia記事の日本語訳を作成することにしました。
過去の記事「Wikipedia 英語記事「HIV(ヒト免疫不全ウイルス)の構造とゲノム」の日本語訳 その1」もご参考のこと。
Genome organization / ゲノム構造
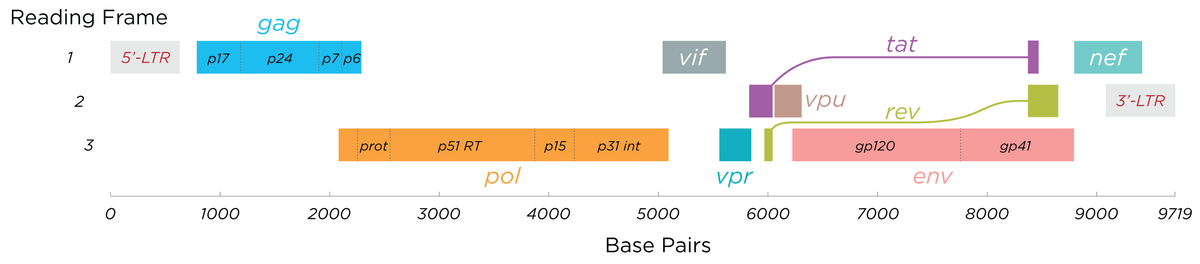
HIVは、すべてのレトロウイルスに見られる構造タンパク質をコードするいくつかの主要な遺伝子と、HIVに特有のいくつかの非構造(アクセサリー)遺伝子を有している*1。 HIVゲノムには、15種類のウイルスタンパク質をコードする、9つの遺伝子が含まれる*2。 これらは、Gagと呼ばれるビリオン内部のタンパク質、群特異抗原、ウイルス酵素(Pol、ポリメラーゼ)、またはビリオンenv(エンベロープ)の糖タンパク質を生成するポリタンパク質として合成される*3。 これらに加えて、HIVは、ある種の制御的および補助的な機能を持つタンパク質もコードしている*4。 HIV-1には、2つの重要な制御因子TatとRevがある。 また、Nef、Vpr、Vif、Vpuなどの重要なアクセサリータンパク質は、特定の組織では複製に必須ではない*5。 gag遺伝子はウイルスの基本的な物理的基盤を提供して、polはレトロウイルスが繁殖する基本的なメカニズムを提供する。その他はHIVが宿主細胞に侵入して繁殖を促進するのを助ける。 突然変異によって変化することもあるが、tevを除くこれらの遺伝子は、HIVの既知のすべての変異体に存在する。
HIVは、10kb未満のゲノムから9つの異なる遺伝子産物を得るために、選択的スプライシングの洗練されたシステムを駆使する*6。 HIVは、gagとpol前駆体をコードする9.2kbの非スプライスゲノム転写物を持つ。 つまりは、 env、Vif、VprおよびVpuをコードするシングルスプライシングされた4.5kbのmRNAと、Tat、RevおよびNefをコードするマルチプルスプライシングされた2kbのmRNAを有する*7。
Viral structural proteins / ウイルス構造タンパク質
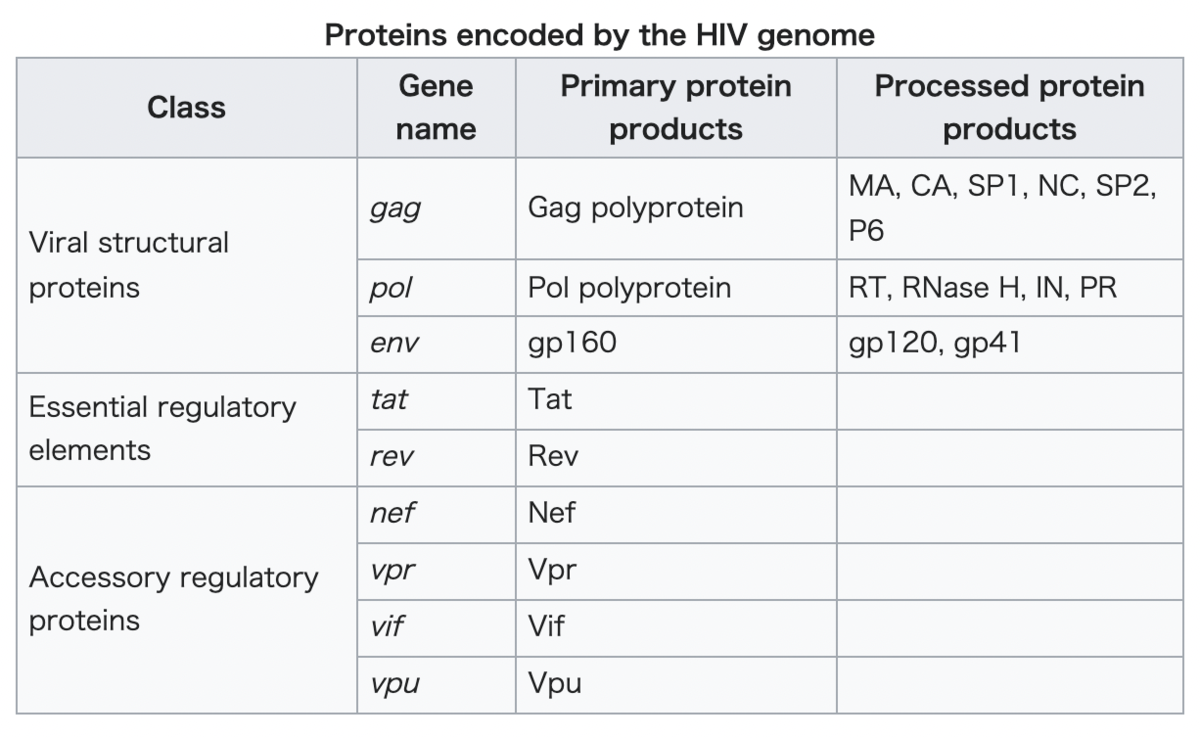
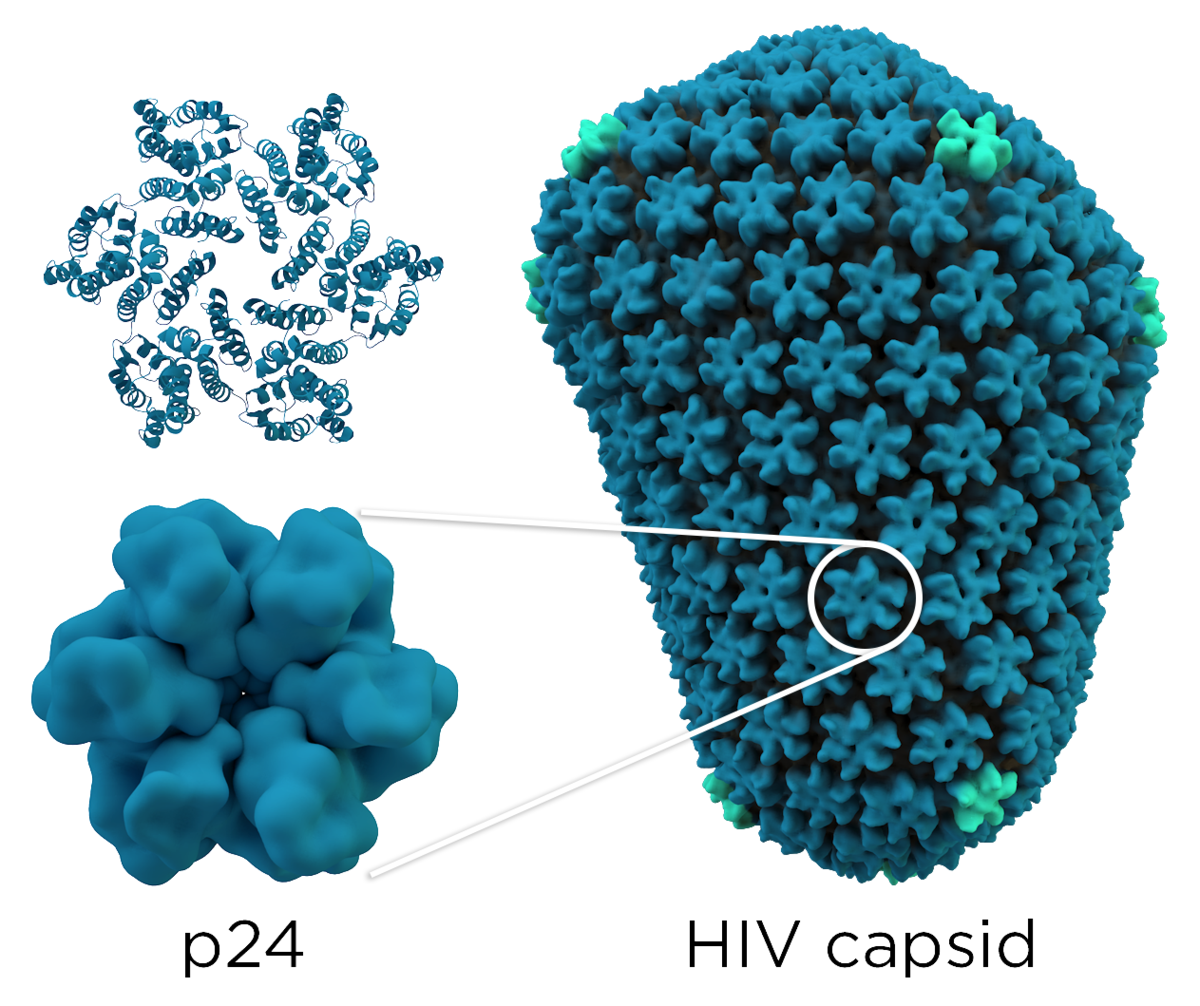
gag(群特異抗原)は、前駆体のgagポリタンパク質をコードし、成熟中にウイルスのプロテアーゼによって、MA(マトリックスタンパク質、p17)、CA(キャプシドタンパク質、p24)、SP1(スペーサーペプチド1、p2)、NC(ヌクレオカプシドタンパク質、p7)、SP2(スペーサーペプチド2、p1)およびP6タンパク質へと分解される*8。
polは、ウイルス酵素の逆転写酵素(RT)とRNase H、インテグラーゼ(IN)、およびHIVプロテアーゼ(PR)をコードする*9。 HIVプロテアーゼは、前駆体Gagポリタンパク質を切断して構造タンパク質を生成するために必要である。RTは、RNA鋳型からDNAを逆転写するために必要である。INは、二本鎖のウイルスDNAを宿主ゲノムに統合するために必要である*10。
env(エンベロープ)は、gp160をコードし、宿主細胞の小胞体内で宿主のプロテアーゼであるfurinによって切断される。 翻訳後の処理により、表面糖タンパク質であるgp120またはSUが生成される。 これは、リンパ球に存在するCD4受容体に結合し、gp41またはTMはウイルスエンベロープに埋め込まれて、ウイルスが標的細胞に付着して融合できるようにする*11 *12。
Essential regulatory elements / 必須の規制要素
tat (HIV trans-activator) は、ウイルスゲノムRNAの逆転写を制御し、ウイルスmRNAを効率的に合成し、感染細胞からのビリオンの放出を制御する重要な役割を果たす*13。 Tatは、72アミノ酸の1エクソンTatと86-101アミノ酸の2エクソンTatとして発現しており、HIV感染初期に重要な役割を果たす。 Tat (14-15 kDa) は、5' LTR 領域付近の膨らんだゲノム RNA のステムループ二次構造に結合し、トランス活性化応答要素 (TAR, trans-activation response element) を形成する*14 *15。
rev (ビリオンタンパク質の発現制御因子): Revタンパク質は、アルギニンに富んだRNA結合モチーフを介してウイルスゲノムに結合し、NLS(核局在シグナル)としても機能し、ウイルス複製時に細胞質から核に輸送されるのに必要である*16。 Revは、HIV Rev response element (RRE) として知られる、TatとRevのコーディングエクソンを分離するイントロンに位置するmRNA envに存在する複雑なステムループ構造を認識する*17 *18。 Revは、主要なウイルスタンパク質の合成に重要であり、それゆえウイルス複製に不可欠である*19。
Accessory regulatory proteins / アクセサリー制御タンパク質
vpr (レンチウイルスタンパク質 R): Vprは、ウイルスに関連した、核・細胞質シャトリング制御タンパク質である*20。ウイルスの複製、特に、前統合複合体の核内取り込みに重要な役割を果たすと考えられている。また、Vprは宿主細胞の細胞周期をG2期で停止させるようである。 この停止は、宿主のDNA修復機構を活性化させ、ウイルスDNAの統合を可能にするかもしれにあ*21。 HIV-2およびSIVは、Vpxと呼ばれるVprに関連するタンパク質をさらにコードしており、Vprと連携して機能する*22。
vif: Vifは、高度に保存された23kDaのリン酸化タンパク質で、細胞種に依存するHIV-1ビリオンの感染性に重要である。 HIV-1は、リンパ球、マクロファージ、特定のヒト細胞株において感染性ウイルスを合成するために、Vifを必要としていることが判明している。 HeLa細胞やCOS細胞などでは、同じプロセスのためにVifを必要としない。
nef: Nef(ネガティブファクター)は、N末端がミリストイル化された膜結合型リン酸化タンパク質である。 ウイルスの複製サイクルにおいて、複数の機能に関与している。 細胞のアポトーシスに重要な役割を果たし、ウイルスの感染性を高めると考えられる。
vpu (Virus protein U): Vpuは、HIV-1に特異的である。 クラスIのオリゴマー型膜蛋白質で、多くの生物学的機能を持つ。 Vpuは、ユビキチンプロテアソーム経路を介したCD4分解や、感染細胞からのビリオンの放出に関与している。
tev:tev遺伝子は数少ないHIV-1分離株にしか存在しない。 tat、env、rev遺伝子の一部が融合したもので、tatの特性の一部を持つが、 revの特性はほとんど持たないタンパク質をコードしている*23。
RNA secondary structure / RNAの二次構造
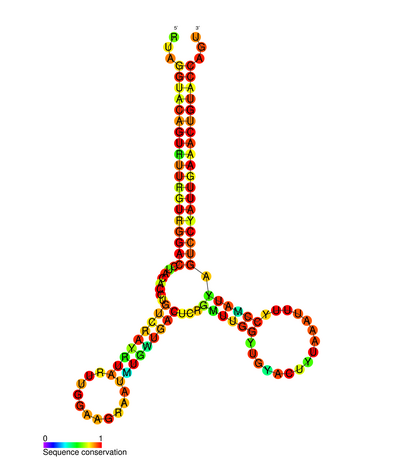
HIV RNAゲノムには、いくつかの保存された二次構造エレメントが同定されている。 5'UTR構造は、小さなリンカーでつながれた一連のステムループ構造からなる。 これらのステムループ(5'から3')には、トランス活性化領域(TAR)エレメント、 5'ポリアデニル化シグナル [poly(A)]、PBS、DIS、メジャーSD、およびゲノムの5'末端にあるψヘアピン構造、 env遺伝子内のHIV Rev response element(RRE)などが含まれる。 同定された別のRNA構造は、gag stem loop 3 (GSL3) で、ウイルスのパッケージングに関与していると考えられている*24 *25。 RNA二次構造は、HIVプロテアーゼや逆転写酵素の機能を変化させ、HIVのライフサイクルに影響を与えると提案されているが、特定されたすべてのエレメントで機能が割り当てられたわけではない*26。
SHAPE解析によって決定されたRNA二次構造は、3つのステムループを含み、HIVプロテアーゼ遺伝子と逆転写酵素遺伝子の間に位置することが示された。 このシス制御RNAは、HIVファミリー全体で保存されていることが示されており、ウイルスのライフサイクルに影響を及ぼすと考えられる*27。
V3 loop / V3ループ
第3可変ループ(V3ループ)は、ヒト免疫不全ウイルスの一部または領域である。 エンベロープ糖タンパク質gp120のV3ループは、HIV株によって、CCR5細胞やCXCR4細胞のような標的ヒト免疫細胞上のサイトカイン受容体に結合することによって、ヒト免疫細胞に感染することができる*28。 エンベロープ糖タンパク質(Env)gp120/41は、HIV-1の細胞への侵入に必須である。 エンベロープは、HIV-1感染者の治療薬の分子標的であり、エイズワクチンの免疫原の一つである。 しかし、機能的なEnvの3量体の構造は不明であった*29。
*1:Mushahwar IK (2007). "Human Immunodeficiency Viruses: Molecular Virology, pathogenesis, diagnosis and treatment". Perspectives in Medical Virology. 13: 75–87. doi:10.1016/S0168-7069(06)13005-0. ISBN 9780444520739.
*2:Li G, Piampongsant S, Faria NR, Voet A, Pineda-Peña AC, Khouri R, Lemey P, Vandamme AM, Theys K (February 2015). "An integrated map of HIV genome-wide variation from a population perspective". Retrovirology. 12 (1): 18. doi:10.1186/s12977-015-0148-6. PMC 4358901. PMID 25808207.
*3:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*4:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*5:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*6:Feinberg Mark B, Greene Warner C (1992). "Molecular Insights into human immunodeficiency virus type1 pathogenesis". Current Opinion in Immunology. 4 (4): 466–474. doi:10.1016/s0952-7915(06)80041-5. PMID 1356348.
*7:Feinberg Mark B, Greene Warner C (1992). "Molecular Insights into human immunodeficiency virus type1 pathogenesis". Current Opinion in Immunology. 4 (4): 466–474. doi:10.1016/s0952-7915(06)80041-5. PMID 1356348.
*8:King Steven R (1994). "HIV: Virology and Mechanisms of disease". Annals of Emergency Medicine. 24 (3): 443–449. doi:10.1016/s0196-0644(94)70181-4. PMID 7915889.
*9:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*10:Mushahwar IK (2007). "Human Immunodeficiency Viruses: Molecular Virology, pathogenesis, diagnosis and treatment". Perspectives in Medical Virology. 13: 75–87. doi:10.1016/S0168-7069(06)13005-0. ISBN 9780444520739.
*11:Mushahwar IK (2007). "Human Immunodeficiency Viruses: Molecular Virology, pathogenesis, diagnosis and treatment". Perspectives in Medical Virology. 13: 75–87. doi:10.1016/S0168-7069(06)13005-0. ISBN 9780444520739.
*12:King Steven R (1994). "HIV: Virology and Mechanisms of disease". Annals of Emergency Medicine. 24 (3): 443–449. doi:10.1016/s0196-0644(94)70181-4. PMID 7915889.
*13:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*14:Montagnier L (1999). "Human Immunodeficiency Viruses (Retroviridae)". Encyclopedia of Virology (2nd ed.). pp. 763–774.
*15:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*16:ビリオンタンパク質の発現制御因子
*17:Montagnier L (1999). "Human Immunodeficiency Viruses (Retroviridae)". Encyclopedia of Virology (2nd ed.). pp. 763–774.
*18:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*19:要出典
*20:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*21:Montagnier L (1999). "Human Immunodeficiency Viruses (Retroviridae)". Encyclopedia of Virology (2nd ed.). pp. 763–774.
*22:Votteler J, Schubert U (2008). "Human Immunodeficiency Viruses: Molecular Biology". Encyclopedia of Virology (3rd ed.). pp. 517–525.
*23:Benko DM, Schwartz S, Pavlakis GN, Felber BK (June 1990). "A novel human immunodeficiency virus type 1 protein, tev, shares sequences with tat, env, and rev proteins". Journal of Virology. 64 (6): 2505–18. doi:10.1128/JVI.64.6.2505-2518.1990. PMC 249426. PMID 2186172.
*24:Damgaard CK, Andersen ES, Knudsen B, Gorodkin J, Kjems J (February 2004). "RNA interactions in the 5' region of the HIV-1 genome". Journal of Molecular Biology. 336 (2): 369–79. doi:10.1016/j.jmb.2003.12.010. PMID 14757051.
*25:Rong L, Russell RS, Hu J, Laughrea M, Wainberg MA, Liang C (September 2003). "Deletion of stem-loop 3 is compensated by second-site mutations within the Gag protein of human immunodeficiency virus type 1". Virology. 314 (1): 221–8. doi:10.1016/S0042-6822(03)00405-7. PMID 14517075.
*26:要引用
*27:Wang Q, Barr I, Guo F, Lee C (December 2008). "Evidence of a novel RNA secondary structure in the coding region of HIV-1 pol gene". RNA. 14 (12): 2478–88. doi:10.1261/rna.1252608. PMC 2590956. PMID 18974280.
*28:"The interactions of the gp120 V3 loop of different HIV-1 strains with the potent anti-HIV human monoclonal antibody 447-52D". Weizmann Institute of Science: Department of Structural Biology. Archived from the original on 2007-07-18. Retrieved 2017-04-18.
*29:Takeda S, Takizawa M, Miyauchi K, Urano E, Fujino M, Murakami T, Murakami T, Komano J (June 2016). "Conformational properties of the third variable loop of HIV-1AD8 envelope glycoprotein in the liganded conditions". Biochemical and Biophysical Research Communications. 475 (1): 113–8. doi:10.1016/j.bbrc.2016.05.051. PMID 27178216.